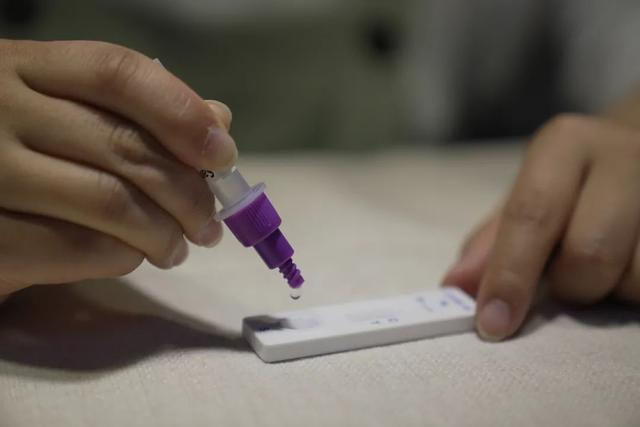
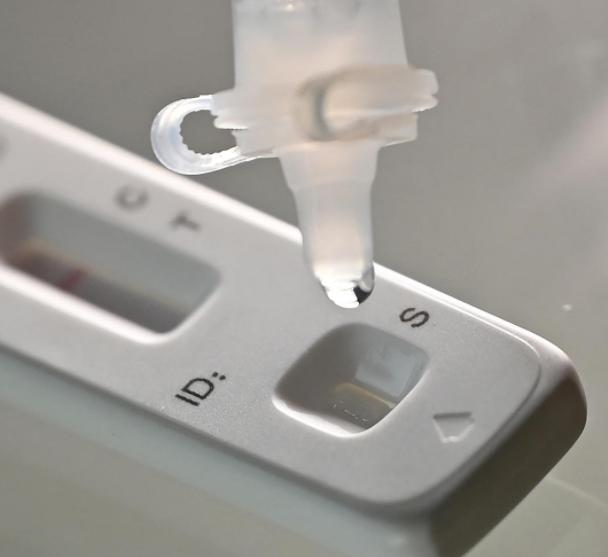
Vào ngày 12 tháng 3th 2022, cácNMPA (SFDA) ra thông báo chấp thuận việc thay đổi đơn đăng ký tự kiểm tra sản phẩm kháng nguyên COVID-19 của Nanjing Vazyme BiotechCông ty Trách Nhiệm Hữu Hạn, Công nghệ kỹ thuật sinh học Jinwofu Bắc KinhCông ty Trách Nhiệm Hữu Hạn, Thâm Quyến Huada Yinyuan Pharmaceutical Technology Co., Ltd, Quảng Châu Wondfo Biotech Co., Ltd vàBeijing Savant Biotechnology Co., ltd(Huaketai).Năm sản phẩm tự kiểm tra kháng nguyên COVID-19 đã được đưa ra.
Vào ngày 11 tháng 3 năm 2022, NHC đã thông báo rằng, để tối ưu hóa hơn nữa chiến lược thử nghiệm Coronavirus mới và phục vụ nhu cầu phòng chống và kiểm soát COVID-19, Nhóm Toàn diện của Cơ chế chung phòng và kiểm soát của Hội đồng Nhà nước đã quyết định bổ sung thử nghiệm kháng nguyên đối với thử nghiệm axit nucleic và thực hiện “Giao thức ứng dụng để phát hiện kháng nguyên mới của Coronavirus (Thử nghiệm)”
Giao thức chỉ định dân số áp dụng để kiểm tra kháng nguyên:
Đầu tiên, những người đến khám tại các cơ sở y tế ban đầu và có các triệu chứng như đường hô hấp và sốt trong vòng 5 ngày kể từ khi có triệu chứng;
Thứ hai, nhân viên quan sát kiểm dịch, bao gồm quan sát kiểm dịch tại nhà, tiếp xúc gần và tiếp xúc phụ, quan sát kiểm dịch nhập cảnh, nhân viên khu vực quản thúc và khu vực kiểm soát;
Thứ ba là cộng đồng cư dân có nhu cầu tự phát hiện kháng nguyên.
Lời khuyên: Phát hiện kháng nguyên là một bổ sung quan trọng của việc phát hiện axit nucleic, nhưng kết quả của quá trình tự phát hiện kháng nguyên không thể được sử dụng làm cơ sở để chẩn đoán nhiễm trùng
Thời gian đăng: 22-03-2022